Washington, ngày 13/4/2026 – Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) hôm nay đã chính thức phê duyệt thuốc mới mang tên Lecanemab-2 (tên thương mại dự kiến là Leqembi Ultra) để điều trị bệnh Alzheimer ở giai đoạn sớm.
Theo kết quả thử nghiệm lâm sàng giai đoạn 3 được công bố, thuốc làm chậm tốc độ suy giảm nhận thức và chức năng hàng ngày của người bệnh lên đến 35% so với nhóm dùng placebo sau 18 tháng điều trị. Đây là mức cải thiện lớn nhất từ trước đến nay của một loại thuốc kháng amyloid.
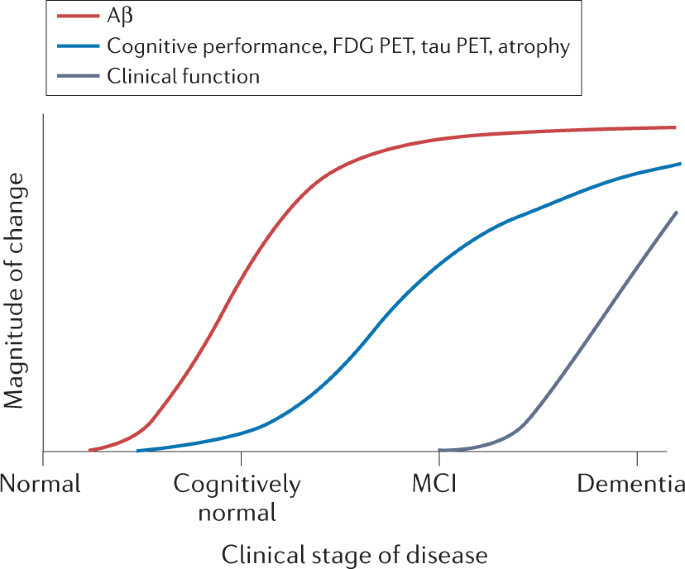
Hình minh họa não bộ Alzheimer với tiến triển từ giai đoạn bình thường đến sa sút trí tuệ, nổi bật vùng tích tụ amyloid plaque – mục tiêu chính của thuốc mới Lecanemab-2 (Leqembi Ultra) vừa được FDA phê duyệt — Nguồn: Nature Reviews Neurology
Ý nghĩa của phê duyệt
Thuốc được chỉ định cho bệnh nhân Alzheimer giai đoạn nhẹ và tiền lâm sàng (có tích tụ amyloid nhưng chưa có triệu chứng rõ rệt).
Đây là lần thứ hai FDA phê duyệt một thuốc kháng amyloid theo cơ chế “accelerated approval” sau Leqembi (2023).
Các chuyên gia đánh giá đây là bước tiến lớn, mở ra hy vọng mới cho hơn 6,9 triệu người Mỹ đang sống chung với Alzheimer.
Phản ứng từ chuyên gia Tiến sĩ Maria Carrillo, Giám đốc Khoa học Alzheimer’s Association: “Đây là kết quả quan trọng nhất trong 20 năm qua. Làm chậm tiến triển 35% có nghĩa là người bệnh có thể giữ được khả năng tự chăm sóc bản thân lâu hơn, giảm gánh nặng cho gia đình và hệ thống y tế.”
Tác động thực tế Thuốc sẽ được bán với giá khoảng 26.500 USD/năm (sau khi đã giảm). Medicare và các công ty bảo hiểm lớn cho biết đang xem xét bao phủ chi phí cho bệnh nhân đủ điều kiện.
FDA yêu cầu tiếp tục theo dõi an toàn lâu dài, đặc biệt là nguy cơ phù não và xuất huyết não – tác dụng phụ đã được ghi nhận ở một số bệnh nhân.